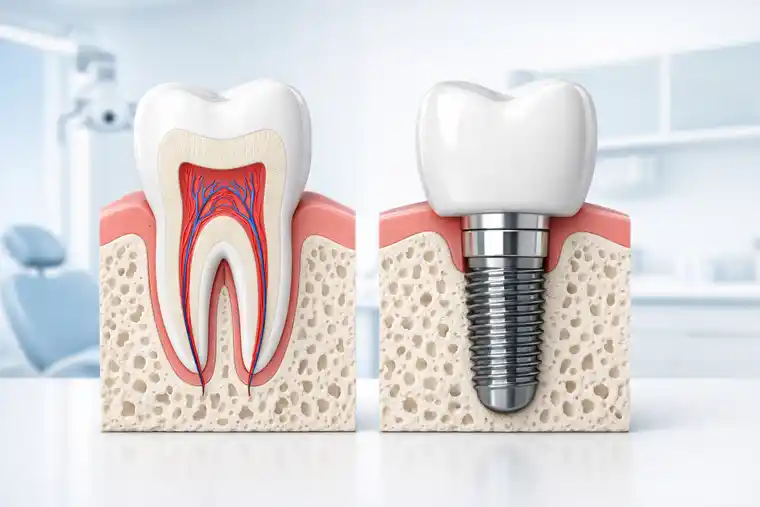
Terapia con células madre para la isquemia crónica: Una nueva vía para salvar extremidades
Caso clínico y molecular de revascularización tisular con ArtAssist y G-CSF en isquemia crónica Por DARWIN ETON MD, FACS, DFSVS, ORCID# 0000-0001-6732-1413 Director Científico y Médico, Vasogenesis Inc, 32 Marshal St., Boston, MA 02446, EE. UU.
Información sobre la financiación: Fundación Warren H. y Clara Cole; Cures Within Reach; Departamento de Cirugía Universidad de Chicago
Tabla de contenidos
Por qué falla la neovascularización en la isquemia crónica y cómo solucionarlo
Se probó una estrategia terapéutica basada en células madre que pretende mejorar la cinética de la neovascularización (NV) en pacientes con isquemia crónica. Se diseñó para superar los obstáculos hemodinámicos y celulares a la NV que surgen durante la evolución de la enfermedad arterial. https://doi.org/10.1002/term.3284
La NV es el mecanismo normal por el que la Naturaleza mejora el flujo sanguíneo en el tejido isquémico caudal a la enfermedad oclusiva arterial. Los biólogos vasculares y los hematólogos han dilucidado muchos de los mecanismos implicados. Estos contribuyeron al desarrollo de nuestra estrategia.
Los dos pilares de la reparación vascular: Arteriogénesis y Angiogénesis
La NV puede dividirse en dos procesos.
La arteriogénesis es el crecimiento del diámetro y el número de arterias colaterales. Se inicia por el aumento de la tensión de cizallamiento en las células endoteliales que recubren la superficie luminal de las ramas arteriales (calles laterales) que se conectan en red alrededor de una arteria grande ocluida (avenida principal).
La angiogénesis es el crecimiento inducido por la hipoxia de las arteriolas y capilares que suministran el flujo sanguíneo nutritivo oxigenado a las células del tejido isquémico, y de las vénulas que eliminan los productos de desecho del metabolismo. Angiográficamente, la arteriogénesis se visualiza como arterias colaterales en forma de «sacacorchos», y la angiogénesis aparece como un rubor en el tejido. Ambas aceleran el tránsito del contraste a través del tejido isquémico.
Salvamento de extremidades sin cirugía en Estambul: Un gran avance en la terapia de compresión
La NV no se produce de forma eficaz porque surgen varios obstáculos. La isquemia envenena el microentorno biosintético al dificultar el suministro de flujo sanguíneo nutritivo oxigenado y la eliminación de los metabolitos tóxicos.
Al superarse la capacidad de amortiguación local, la acidosis resultante acelera la desnaturalización de las proteínas y altera la permeabilidad de la membrana celular. Una deficiencia de las estrategias diseñadas hasta la fecha para promover la NV es que no mejoran primero el bioentorno isquémico.
Por otra parte, estas estrategias no abordaron la tensión de cizallamiento endotelial gravemente atenuada necesaria para iniciar la activación de las células endoteliales que conduce a la arteriogénesis. Esto es especialmente importante en pacientes con enfermedad oclusiva arterial multinivel que atenúa gravemente el flujo arterial colateral.
Además, las células afectadas del tejido isquémico segregan importantes proteínas de señalización (por ejemplo, SDF-1α) destinadas a ser transportadas por el retorno venoso a los nichos de células progenitoras de todo el cuerpo para reclutar estas células salutíferas de vuelta al endotelio activado.
El flujo sanguíneo deficiente no sólo perjudica la síntesis de proteínas de señalización y la diseminación, sino que también atenúa la entrega de cualquier célula movilizada de vuelta al tejido diana. La resistencia de la enfermedad oclusiva arterial simplemente provoca la desviación del flujo sanguíneo y la deposición de células en cualquier otro lugar que no sea el tejido isquémico.
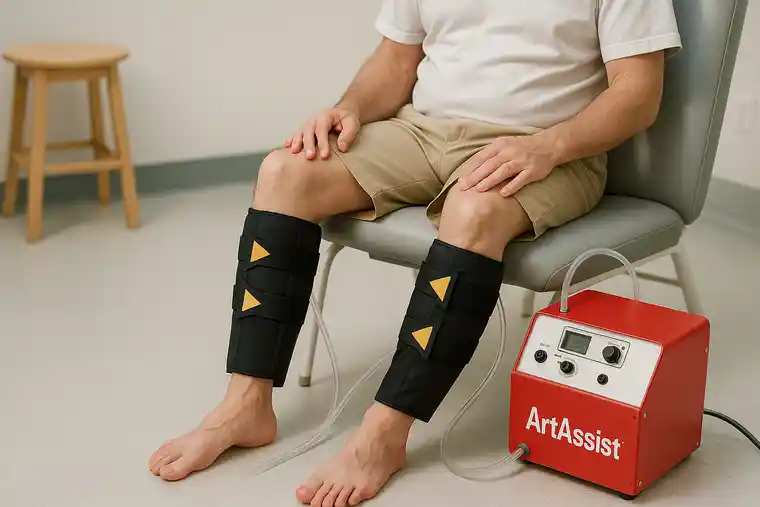
Cómo favorece la neovascularización el dispositivo ArtAssist
Mejorar la afluencia arterial nutritiva oxigenada, eliminar los metabolitos tóxicos, proporcionar el estímulo endotelial del esfuerzo cortante y mejorar la difusión y el suministro de proteínas y células beneficiosas es cada vez más importante cuanto más alejado del corazón esté el tejido isquémico. En pacientes con isquemia crónica de las extremidades (ICTM) utilizamos un dispositivo que administraba una fuerza mecánica pulsátil externamente a la pantorrilla, el tobillo y el pie para hacer frente a todos estos obstáculos (dispositivo ArtAssist, ACI Medical (San Marcos, CA)).
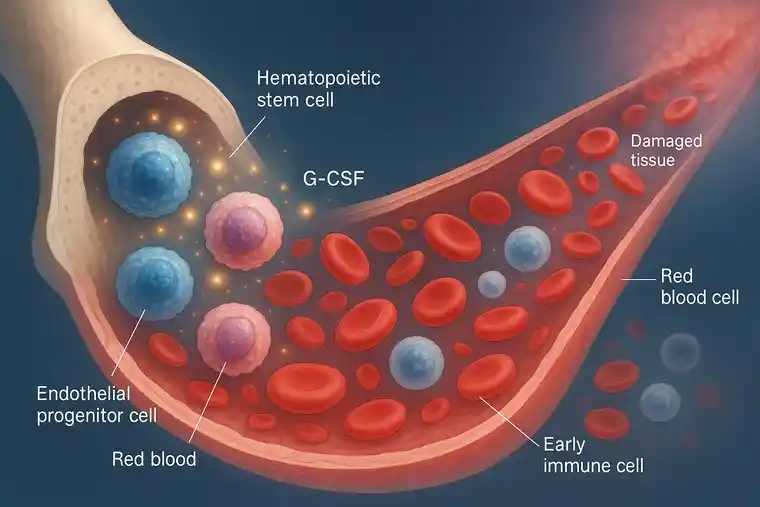
Movilización de células madre con G-CSF: aumento natural del flujo sanguíneo
La NV está orquestada en gran parte por elementos celulares derivados de la línea de células progenitoras y de células inflamatorias (como los monocitos).
En pacientes con edad avanzada, diabetes y enfermedad vascular grave, un obstáculo importante para la NV es la disminución del número y la función de las células progenitoras circulantes. Por lo tanto, no basta con mejorar el microentorno biosintético para mejorar la NV, a menos que también se pueda mejorar la disponibilidad de células progenitoras y monocitos saludables.
Decidimos abordar este obstáculo con el factor estimulante de colonias de granulocitos (G-CSF), utilizado habitualmente en la terapia con células madre para movilizar células hematopoyéticas y progenitoras y amplificar el sistema inmunitario. Utilizamos Neupogen (amgen Inc) en una dosimetría novedosa (7-10 mcg/kg) cada 72 horas durante 10 dosis en pacientes con CLTI que llevaban el dispositivo ArtAssist diariamente durante un mínimo de 3 horas (mientras estaban sentados).
Recuperación de extremidades en pacientes sin opción de tratamiento
Los pacientes con ITCL tratados se consideraron ITCL «sin opción» tras agotar las opciones de revascularización tradicionales (bypass quirúrgico, angioplastia, aterectomía, recanalización con láser).
Se les trató en lugar de una amputación mayor. La recuperación de la extremidad y la cicatrización de las heridas isquémicas en los primeros pacientes tratados condujeron a la documentación angiográfica de arteriogénesis, angiogénesis y, lo más sorprendente, a la evidencia de recanalización de una oclusión arterial segmentaria previamente documentada.
Esto condujo a la medición de los niveles plasmáticos de plasmina (causante de la fibrinólisis) y de productos de degradación de la fibrina (producidos por el trombo sometido a fibrinólisis), junto con una batería de proteínas proangiogénicas. Estos ensayos inmunoabsorbentes ligados a enzimas (ELISA) confirmaron que, efectivamente, nuestro enfoque basado en células madre conducía a la NV y a la superación de otro obstáculo importante para la NV: el trombo crónico(https://doi.org/10.1002/term.3284).
Pruebas clínicas y moleculares de la neovascularización
Una revisión detallada de los participantes celulares y moleculares en la NV y de su relevancia para esta prometedora estrategia de NV está disponible en https://doi.org/10.1016/j.jvsvi.2025.100190, que destaca cómo cada uno de los participantes celulares (endotelio, células progenitoras, neutrófilos, monocitos, etc.) contribuye a explicar las observaciones de los ensayos moleculares y de citometría detallados que realizamos en nuestros pacientes.
Estos datos corroboraron las pruebas hemodinámicas y angiográficas de la mejora del flujo sanguíneo y subrayaron lo importante que es medir el impacto molecular de una terapia celular (algo de lo que carecían los anteriores ensayos clínicos de NV).
Contra todo pronóstico, los pacientes con ITCL «sin opción» lograron salvar la extremidad. Sin embargo, existe una clara diferencia entre la rapidez con la que nuestro tratamiento mejora el flujo sanguíneo y la velocidad de deterioro de la enfermedad vascular avanzada.
Aunque la recuperación de la extremidad se basa en la mejora del flujo sanguíneo (el objetivo de nuestra estrategia), también depende del cuidado avanzado y diligente de las heridas, el tratamiento de la sepsis, el desbridamiento, la nutrición, las comorbilidades, el cumplimiento terapéutico y la evitación de traumatismos.
Como tal, la aplicación de una estrategia de NV es probablemente mejor en las primeras fases de la isquemia crónica, antes de realizar cualquier intervención tradicional y antes de que las heridas isquémicas se agraven tanto que la sepsis requiera un desbridamiento extenso. Cuanto más se intervenga, ya sea para revascularizar con medios tradicionales o para tratar obligatoriamente la herida quirúrgica, más alterada estará la anatomía.
La inflamación aguda y la fibrosis postoperatoria son barreras potenciales para la NV. Un buen ejemplo de ello es que los neutrófilos en el contexto de una inflamación aguda son protrombóticos y antiangiogénicos, mientras que en ausencia de inflamación aguda los neutrófilos tienen capacidad fibrinolítica y proangiogénica.
Esta actividad de los neutrófilos dependiente del contexto es especialmente importante en pacientes tratados con G-CSF, que provoca un aumento transitorio de 5 a 12 veces en el recuento absoluto de neutrófilos.
Por qué fracasan las intervenciones tradicionales en la isquemia crónica
Las intervenciones quirúrgicas y endovasculares tradicionales son costosas e invasivas. Su ventaja, cuando tienen éxito, es el restablecimiento inmediato del flujo.
Su punto débil es la durabilidad, siendo la hiperplasia intimal y la enfermedad recurrente causas no infrecuentes de fracaso a medio (6 meses a 2 años) y largo plazo.
Es importante destacar que la corrección aguda del flujo arterial es eficaz para aliviar los síntomas, pero también detiene la capacidad intrínseca de reparación vascular (NV).
Un cambio de paradigma hacia la revascularización a nivel tisular
Ha llegado la hora de cambiar el enfoque en el tratamiento de la isquemia crónica de las estrategias de revascularización aguda de las grandes arterias a la revascularización a nivel tisular.
Al fin y al cabo, ningún cirujano vascular intervino en el desarrollo y crecimiento de nuestra circulación (a partir de un espermatozoide y un óvulo).
La naturaleza sabe cómo hacerlo y, de hecho, lo hace eficazmente hasta que los obstáculos discutidos superan el proceso.
La superación de los obstáculos restaura el NV, como se observa con las terapias avanzadas con células madre y asistidas por dispositivos, que ofrecen una reparación vascular duradera y biológicamente alineada.
Esta novedosa terapia ambulatoria cuesta una fracción de las intervenciones actuales.

Dr Darwin Eton
MD, FACS, DFSVS, Profesor jubilado de Cirugía Vascular
Distinguido por sus avances en la investigación de las enfermedades vasculares
Acerca del Dr. Darwin Eton
El Dr. Darwin Eton, MD, FACS, DFSVS es catedrático jubilado de cirugía vascular y ex director de programas clínicos avanzados en enfermedades vasculares periféricas. A lo largo de su carrera, el Dr. Eton ha desempeñado un papel decisivo en la remodelación de la forma en que los cirujanos vasculares y los científicos entienden la fisiopatología isquémica, especialmente en el contexto de la terapéutica celular y regenerativa.
Para obtener más información sobre las contribuciones académicas y clínicas del Dr. Eton, consulte la sección de noticias y busque:
«Darwin Eton MD, FACS Honored for Advancing Research in the Management of Vascular Disease»
Si desea profundizar, consulte:
Un artículo reciente de JVS(https://doi.org/10.1016/j.jvsvi.2025.100190)
ofrece un resumen de 2025 de los mecanismos y participantes celulares de la neovascularización y la fibrinolisis.
La gravedad de la isquemia crónica derivada de la progresión de la oclusión arterial multinivel se ve atenuada por la neovascularización (NV). Independientemente de lo inteligentes y refinados que se hayan vuelto nuestros procedimientos quirúrgicos/intervencionistas, el énfasis debe cambiar si realmente nos comprometemos a lograr soluciones duraderas, de bajo riesgo y rentables para nuestros pacientes con isquemia crónica.
Siga leyendo … https://doi.org/10.1002/term.3284
Dirigir la correspondencia a:
Darwin Eton MD FACS DFSVS
198 Garvin Hill Rd
Woodstock VT 05091 USA
[email protected]
Móvil: 857-400-4023
Obtenga su consulta gratuita
- ¿Necesita orientación y tranquilidad?
- Hable con una persona de MedClinics.
- Encontremos juntos al médico perfecto.