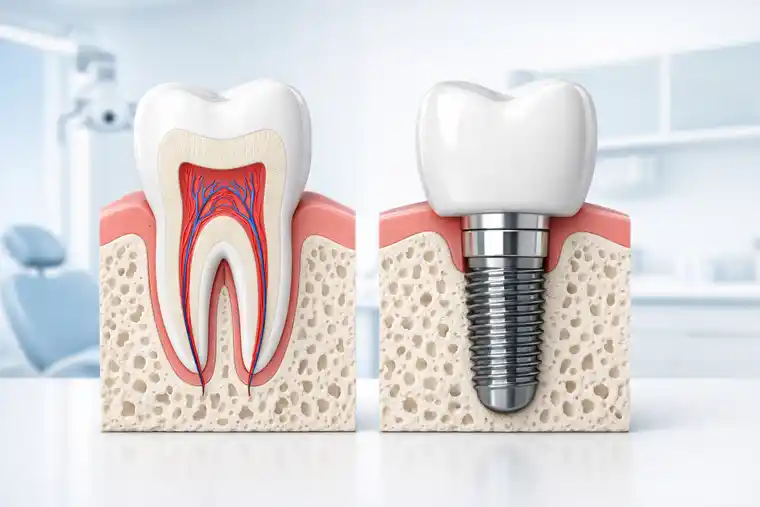
Stammzelltherapie bei chronischer Ischämie: Ein neuer Weg zur Rettung von Gliedmaßen
Ein klinischer und molekularer Fall für Revaskularisierung auf Gewebeebene mit ArtAssist und G-CSF bei chronischer Ischämie
von DARWIN ETON MD, FACS, DFSVS, ORCID# 0000-0001-6732-1413
Chief Science and Medical Officer, Vasogenesis Inc, 32 Marshal St., Boston MA 02446 USA
Informationen zur Finanzierung: Warren H. and Clara Cole Foundation; Cures Within Reach; Abteilung für Chirurgie der Universität Chicago
Warum die Neovaskularisierung bei chronischer Ischämie versagt – und wie man sie beheben kann
Es wurde eine therapeutische Strategie auf der Grundlage von Stammzellen getestet, die darauf abzielt, die Kinetik der Neovaskularisierung (NV) bei Patienten mit chronischer Ischämie zu verbessern. Sie wurde entwickelt, um hämodynamische und zelluläre Hindernisse für die NV zu überwinden, die während der Entwicklung der arteriellen Erkrankung auftreten. https://doi.org/10.1002/term.3284
NV ist der normale Mechanismus, mit dem die Natur den Blutfluss in ischämisches Gewebe kaudal einer arteriellen Verschlusskrankheit verbessert. Gefäßbiologen und Hämatologen haben viele der beteiligten Mechanismen aufgeklärt. Diese haben zur Entwicklung unserer Strategie beigetragen.
Die zwei Säulen der Gefäßreparatur: Arteriogenese und Angiogenese
NV kann in zwei Prozesse unterteilt werden.
Die Arteriogenese ist das Wachstum des Durchmessers und der Anzahl der Kollateralarterien. Sie wird durch die erhöhte Scherbelastung der Endothelzellen ausgelöst, die die Lumenoberfläche von Arterienästen (Seitenstraßen) auskleiden, die sich um eine verschlossene große Arterie (Hauptschlagader) legen.
Unter Angiogenese versteht man das durch Hypoxie ausgelöste Wachstum der Arteriolen und Kapillaren, die die Zellen im ischämischen Gewebe mit sauerstoffreichem, nährstoffreichem Blut versorgen, und der Venolen, die die Abfallprodukte des Stoffwechsels abtransportieren. Angiografisch wird die Arteriogenese als „korkenzieherförmige“ Kollateralarterien dargestellt, und die Angiogenese erscheint als Rötung im Gewebe. Beide beschleunigen den Kontrastmitteltransit durch das ischämische Gewebe.
Rettung von Gliedmaßen ohne Operation in Istanbul: Ein Durchbruch in der Kompressionstherapie
NV scheitert, da eine Reihe von Hindernissen auftreten. Ischämie vergiftet die biosynthetische Mikroumgebung, indem sie die Zufuhr von sauerstoffreichem, nährstoffreichem Blut und die Beseitigung der toxischen Metaboliten beeinträchtigt.
Wenn die lokale Pufferkapazität überschritten wird, beschleunigt die daraus resultierende Azidose die Proteindenaturierung und verändert die Permeabilität der Zellmembran. Ein Manko der bisherigen Strategien zur Förderung der NV ist, dass zunächst die ischämische Bioumgebung nicht verbessert wurde.
Darüber hinaus gingen diese Strategien nicht auf den stark verminderten endothelialen Scherstress ein, der erforderlich ist, um die Aktivierung der Endothelzellen zu initiieren, die zur Arteriogenese führt. Dies ist besonders wichtig bei Patienten mit einer mehrstufigen arteriellen Verschlusskrankheit, die den Kollateralfluss in den Arterien stark einschränkt.
Darüber hinaus sezernieren geschädigte Zellen im ischämischen Gewebe wichtige Signalproteine (z. B. SDF-1α), die durch den venösen Rückfluss zu Nischen von Vorläuferzellen im ganzen Körper transportiert werden sollen, um diese nützlichen Zellen wieder an das aktivierte Endothel zu rekrutieren.
Die schlechte Durchblutung beeinträchtigt nicht nur die Synthese und Verbreitung von Signalproteinen, sondern schwächt auch den Transport der mobilisierten Zellen zurück zum Zielgewebe. Die Resistenz der arteriellen Verschlusskrankheit führt einfach dazu, dass der Blutfluss umgeleitet wird und sich die Zellen überall anders als im ischämischen Gewebe ablagern.
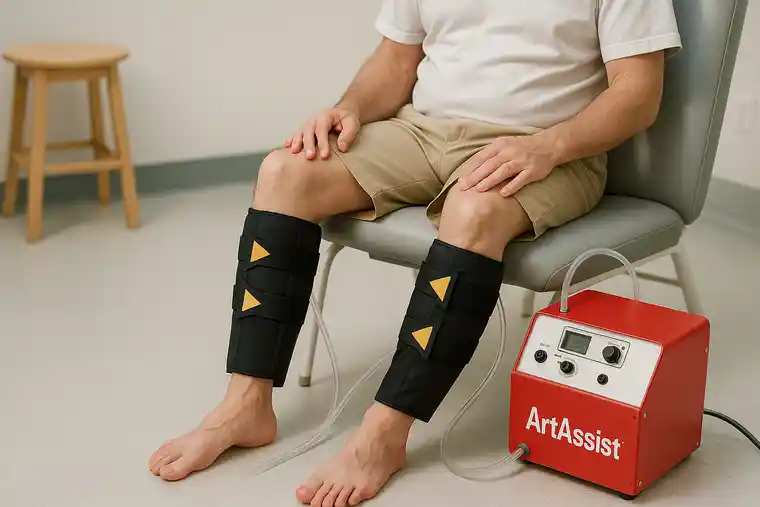
Wie das ArtAssist-Gerät die Neovaskularisierung unterstützt
Die Verbesserung des sauerstoffhaltigen, nährstoffreichen arteriellen Zuflusses, die Beseitigung toxischer Stoffwechselprodukte, die Bereitstellung des endothelialen Scherstressreizes und die Verbesserung der Verbreitung und des Transports heilsamer Proteine und Zellen werden immer wichtiger, je weiter das ischämische Gewebe vom Herzen entfernt ist. Bei Patienten mit chronischer Ischämie der Gliedmaßen (CLTI) haben wir ein Gerät verwendet, das eine pulsierende mechanische Kraft von außen auf den Wadenknöchel und den Fuß ausübt, um all diese Hindernisse zu überwinden (ArtAssist-Gerät, ACI Medical (San Marcos, CA)).
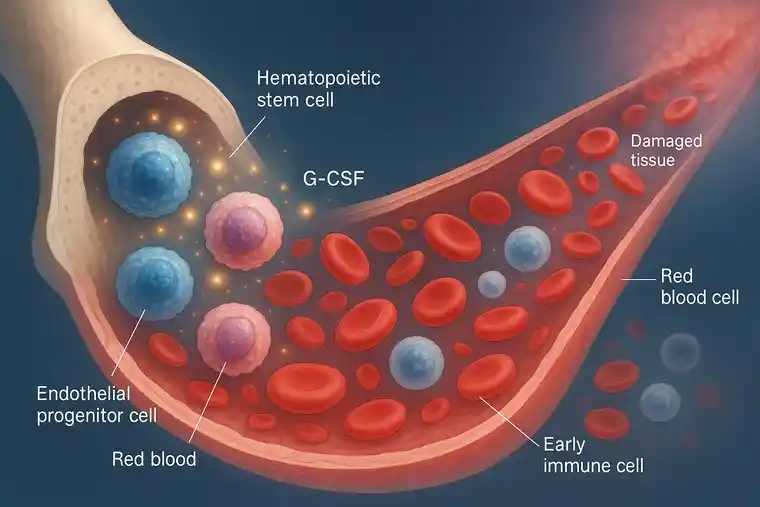
Stammzellmobilisierung mit G-CSF: Natürliche Steigerung des Blutflusses
Die NV wird zu einem großen Teil von zellulären Elementen gesteuert, die aus der Vorläuferzelllinie und aus Entzündungszellen (wie Monozyten) stammen.
Bei Patienten mit fortgeschrittenem Alter, Diabetes und schweren Gefäßerkrankungen ist ein Haupthindernis für die NV die verringerte Anzahl und Funktion der zirkulierenden Vorläuferzellen. Daher reicht eine Verbesserung der biosynthetischen Mikroumgebung allein nicht aus, um die NV zu verbessern, es sei denn, man kann auch die Verfügbarkeit der heilsamen Vorläuferzellen und Monozyten verbessern.
Wir entschieden uns, dieses Hindernis mit dem Granulozyten-Kolonie-stimulierenden Faktor (G-CSF) zu überwinden, der in der Stammzelltherapie üblicherweise zur Mobilisierung von hämatopoetischen Zellen und Vorläuferzellen sowie zur Verstärkung des Immunsystems eingesetzt wird. Wir verwendeten Neupogen (amgen Inc) in einer neuartigen Dosierung (7-10 mcg/kg) alle 72 Stunden für 10 Dosen bei CLTI-Patienten, die das ArtAssist-Gerät täglich für mindestens 3 Stunden (im Sitzen) trugen.
Rettung von Gliedmaßen bei Patienten, die keine Option haben
Bei den behandelten CLTI-Patienten handelte es sich um CLTI-Patienten, die nach Ausschöpfung der herkömmlichen Revaskularisierungsoptionen (chirurgischer Bypass, Angioplastie, Atherektomie, Laser-Rekanalsanierung) als „No-Option“ eingestuft wurden.
Sie wurden anstelle einer größeren Amputation behandelt. Die Rettung der Gliedmaßen und die Heilung der ischämischen Wunden bei den ersten behandelten Patienten führte zur angiografischen Dokumentation von Arteriogenese, Angiogenese und, was am meisten überrascht, zum Nachweis der Rekanalisierung von zuvor dokumentierten segmentalen arteriellen Verschlüssen.
Dies führte zur Messung der Plasmaspiegel von Plasmin (das die Fibrinolyse auslöst) und von Fibrinabbauprodukten (die von Thromben, die der Fibrinolyse unterliegen, produziert werden) sowie einer Reihe von pro-angiogenen Proteinen. Diese ELISA-Tests (Enzyme Linked Immunosorbant Assays) bestätigten, dass unser stammzellgestützter Ansatz in der Tat zu NV führte und ein weiteres großes Hindernis für NV überwand: chronische Thromben(https://doi.org/10.1002/term.3284).
Klinische und molekulare Beweise für Neovaskularisierung
Eine ausführliche Übersicht über die zellulären und molekularen Teilnehmer an der NV und ihre Bedeutung für diese vielversprechende NV-Strategie finden Sie unter https://doi.org/10.1016/j.jvsvi.2025.100190. Darin wird hervorgehoben, wie jeder der zellulären Teilnehmer (Endothel, Vorläuferzellen, neutrophile Granulozyten, Monozyten usw.) zur Erklärung der Beobachtungen aus den detaillierten molekularen und zytometrischen Tests beiträgt, die wir an unseren Patienten durchgeführt haben.
Diese Daten untermauerten die hämodynamischen und angiografischen Hinweise auf eine verbesserte Durchblutung und unterstrichen, wie wichtig es ist, die molekularen Auswirkungen einer Zelltherapie zu messen (was in früheren klinischen NV-Studien nicht möglich war).
„CLTI-Patienten, für die es keine Option gibt, konnten ihre Gliedmaßen retten, obwohl die Chancen sehr gering waren. Es besteht jedoch eindeutig ein Wettlauf zwischen der Geschwindigkeit, mit der unsere Therapie den Blutfluss verbessert, und der Geschwindigkeit der Verschlechterung durch die fortgeschrittene Gefäßerkrankung.
Die Rettung von Gliedmaßen basiert zwar auf einer verbesserten Durchblutung (dem Ziel unserer Strategie), hängt aber auch von einer fortschrittlichen und sorgfältigen Wundpflege, dem Management von Sepsis, Debridement, Ernährung, Komorbiditäten, Compliance und der Vermeidung von Traumata ab.
Daher ist es wahrscheinlich am besten, eine NV-Strategie in den frühen Stadien der chronischen Ischämie anzuwenden, bevor herkömmliche Eingriffe vorgenommen werden und bevor die ischämischen Wunden so schwer werden, dass die Sepsis ein umfassendes Debridement erfordert. Je mehr chirurgische Eingriffe vorgenommen werden, sei es zur Revaskularisierung mit herkömmlichen Mitteln oder zur obligatorischen chirurgischen Wundbehandlung, desto mehr verändert sich die Anatomie.
Akute Entzündungen und postoperative Fibrosen sind potenzielle Hindernisse für NV. Ein gutes Beispiel dafür ist, dass Neutrophile bei akuter Entzündung pro-thrombotisch und anti-angiogen sind, während Neutrophile ohne akute Entzündung fibrinolytische und pro-angiogene Fähigkeiten haben.
Diese kontextabhängige Aktivität der Neutrophilen ist besonders wichtig bei Patienten, die mit G-CSF behandelt werden, das einen vorübergehenden Anstieg der absoluten Neutrophilenzahl um das 5-12fache bewirkt.
Warum traditionelle Interventionen bei chronischer Ischämie versagen
Traditionelle chirurgische und endovaskuläre Eingriffe sind kostspielig und invasiv. Ihr Vorteil ist die sofortige Wiederherstellung des Blutflusses, wenn sie erfolgreich sind.
Ihre Schwäche ist die Langlebigkeit, denn Intimahyperplasie und rezidivierende Erkrankungen sind nicht selten die Ursache für ein Versagen im mittleren (6 Monate bis 2 Jahre) und langfristigen Stadium.
Wichtig ist, dass eine akute Korrektur des arteriellen Blutflusses zwar die Symptome lindert, aber auch die intrinsische Fähigkeit zur Gefäßreparatur (NV) hemmt.
Ein Paradigmenwechsel hin zur Revaskularisierung auf Gewebeebene
Es ist an der Zeit, den Schwerpunkt bei der Behandlung der chronischen Ischämie von der akuten Revaskularisierung großer Arterien auf die Revaskularisierung auf Gewebeebene zu verlagern.
Schließlich war kein Gefäßchirurg an der Entwicklung und dem Wachstum unseres Kreislaufs (aus einem Spermium und einer Eizelle) beteiligt.
Die Natur weiß, wie das geht, und sie tut es auch effektiv, bis die diskutierten Hindernisse den Prozess überwinden.
Durch die Überwindung dieser Hindernisse wird die NV wiederhergestellt, wie dies bei fortschrittlichen stammzell- und gerätegestützten Therapien der Fall ist, die eine dauerhafte, biologisch abgestimmte Gefäßreparatur ermöglichen.
Diese neuartige ambulante Therapie kostet nur einen Bruchteil der heute üblichen Behandlungen.

Dr. Darwin Eton
MD, FACS, DFSVS, Professor für Gefäßchirurgie im Ruhestand
Ausgezeichnet für die Förderung der Forschung im Bereich der Behandlung von Gefäßkrankheiten
Über Dr. Darwin Eton
Dr. Darwin Eton, MD, FACS, DFSVS ist Professor für Gefäßchirurgie im Ruhestand und ehemaliger Leiter fortgeschrittener klinischer Programme für periphere Gefäßerkrankungen. Im Laufe seiner Karriere war Dr. Eton maßgeblich an der Neugestaltung des Verständnisses der Pathophysiologie ischämischer Erkrankungen durch Gefäßchirurgen und Wissenschaftler beteiligt, insbesondere im Zusammenhang mit regenerativen und zellulären Therapeutika.
Wenn Sie mehr über die akademischen und klinischen Beiträge von Dr. Eton erfahren möchten, suchen Sie im Nachrichtenbereich nach:
„Darwin Eton MD, FACS Honored for Advancing Research in the Management of Vascular Disease“.
Wenn Sie tiefer in die Materie einsteigen wollen, lesen Sie bitte:
Ein kürzlich erschienener JVS-Artikel(https://doi.org/10.1016/j.jvsvi.2025.100190)
bietet eine 2025 Zusammenfassung der Mechanismen und zellulären Teilnehmer der Neovaskularisierung und Fibrinolyse.
Die Schwere der chronischen Ischämie, die durch das Fortschreiten eines mehrstufigen arteriellen Verschlusses entsteht, wird durch Neovaskularisation (NV) gemildert. Unabhängig davon, wie ausgeklügelt und raffiniert unsere chirurgischen/interventionellen Verfahren geworden sind, muss sich der Schwerpunkt ändern, wenn wir wirklich dauerhafte, risikoarme und kosteneffektive Lösungen für unsere Patienten mit chronischer Ischämie erreichen wollen.
Lesen Sie weiter … https://doi. org/10.1002/term.3284
Korrespondenzanschrift:
Darwin Eton MD FACS DFSVS
198 Garvin Hill Rd
Woodstock VT 05091 USA
[email protected]
Handy: 1-857-400-4023
Erhalten Sie Ihre kostenlose Beratung
- Brauchen Sie Rat und Sicherheit?
- Sprechen Sie mit einem echten Mitarbeiter von MedClinics!
- Lassen Sie uns gemeinsam den perfekten Arzt finden.